Atrás quedaron los días en los que aparentemente leves infecciones podían terminar con la vida de una persona. Los antibióticos supusieron una revolución en el campo de la medicina. Desde su uso en humanos se estima que han salvado más de 200 millones de vidas, y sólo en EEUU previene más de 200 mil muertes anuales. Pero es posible que en unos años la situación cambie y las bacterias empiecen a ganar la guerra.
El enemigo y nuestras armas
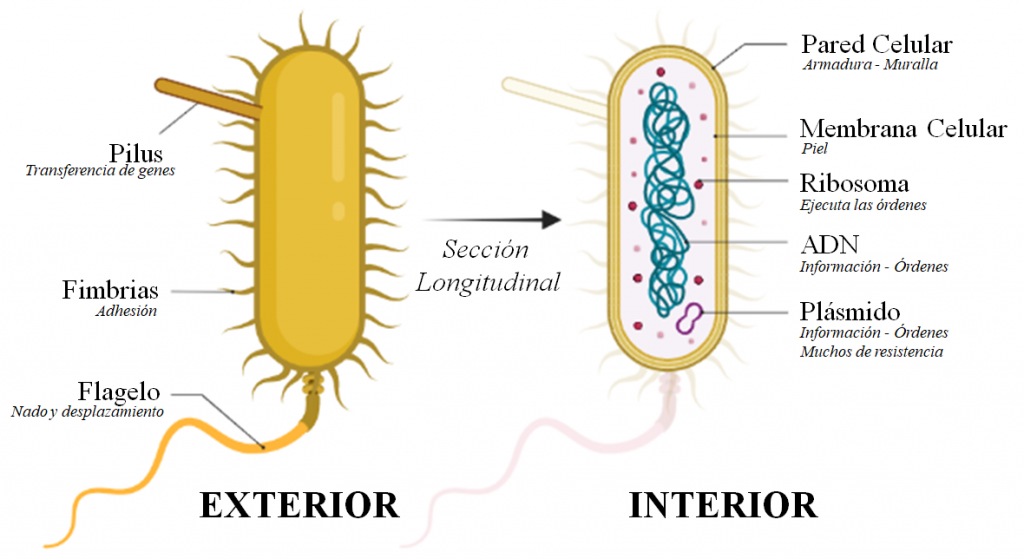
Las bacterias son seres vivos microscópicos prácticamente omnipresentes. Al igual que nosotros están formados por células, pero mientras que un ser humano se compone de cientos de millones de ellas, las bacterias son una única célula en sí misma, es decir, son unicelulares. Esta es su estructura general (figura 1): Una armadura que les da forma y rigidez, llamada pared celular, sin ella muchas explotarían; una piel que regula la entrada y salida de compuestos al interior de la bacteria, llamada membrana celular; el ADN, que al igual que en el resto de los seres vivos contiene la información para mantenerse con vida y reproducirse; los ribosomas, los encargados de leer y ejecutar las órdenes escritas en el ADN; y otras estructuras cuya presencia varía más según la especie bacteriana: flagelos, estructuras en forma de “colita” que les ayudan a nadar y desplazarse; fimbrias, “brazos” que les ayudan a pegarse y agarrarse a superficies y estructuras; pili (pilus, en singular), “arpones” que usan las bacterias para acercarse e intercambiar genes entre bacterias o para “inyectar” directamente ADN; plásmidos, pequeños trozos de ADN que pueden transferirse entre bacterias por medio de pili. En los plásmidos a menudo se encuentran las instrucciones para resistir a los antibióticos.
Tal como se dijo anteriormente, son omnipresentes, lo colonizan todo; están en cualquier superficie natural o artificial, sobre nuestra piel, alimentos, ropa, mascotas, e incluso en nuestro interior. Pero pese a su mala fama, no todas provocan enfermedades, muchas son inocuas (bacterias comensales) e incluso otras nos ayudan a mantenernos con vida (simbióticas) en una maravillosa y compleja relación biológica. Sin ellas, por ejemplo, no podríamos digerir los alimentos vegetales y no podríamos absorber las vitaminas que van en ellos. Se estima que sobre nosotros habitan unos 100 billones de bacterias, todas ellas forman el llamado microbioma humano, un mundo aún poco conocido en el que los científicos están fijando su atención en los últimos años debido a su gran importancia.
Pero cuando las bacterias patógenas, aquellas que causan enfermedades, ganan protagonismo, para mantenerlas a raya y a nosotros sanos, tenemos los antibióticos (AB); fármacos con la capacidad de matar bacterias. Éstos son uno de los pilares de la medicina moderna. Su uso ha reducido la mortalidad y aumentado la esperanza de vida de forma considerable. Además, son esenciales para la realización segura de procedimientos como cirugías y terapias contra el cáncer. Sin ellos, incluso procesos en apariencia sencillos como la extracción de una muela podrían poner en riesgo la vida de un paciente. Además de su uso en la medicina humana, también son importantes para la industria alimentaria, tanto animal como vegetal, y en la veterinaria. Evitan enfermedades en granjas de animales y ayudan a que los campos de cultivo sean más productivos.
Podemos clasificar los AB en función de su diana (Figura 1). Los AB más empleados son aquellos que atacan a la pared celular (muralla) de las bacterias. Como ejemplo tenemos la penicilina, el primer AB descubierto. La penicilina evita que las moléculas de peptidoglicano (los ladrillos de la pared celular) puedan pegarse, y por lo tanto la muralla no se pueda formar provocando que las bacterias exploten y mueran. Otros atacan a los ribosomas, haciendo que no se puedan llevar a cabo las órdenes del ADN; otros directamente al ADN; otros atacan a la membrana bacteriana, la piel de las bacterias, etc.
Ellos también saben defenderse
Si algo nos ha enseñado Darwin es que la biología y la evolución son una carrera armamentística y de adaptación. Por cada arma que crea un ser vivo para defenderse de otro, se genera un contraataque para la supervivencia o por lo contrario la desaparición de la especie atacada. Las bacterias, como seres vivos que son, también se adaptan y evolucionan, y uno de los mecanismos para su adaptación a vivir en seres que consumen AB es la generación de resistencias a estos compuestos. Estas resistencias pueden clasificarse en estos 3 grupos de estrategias (ver figura 2):
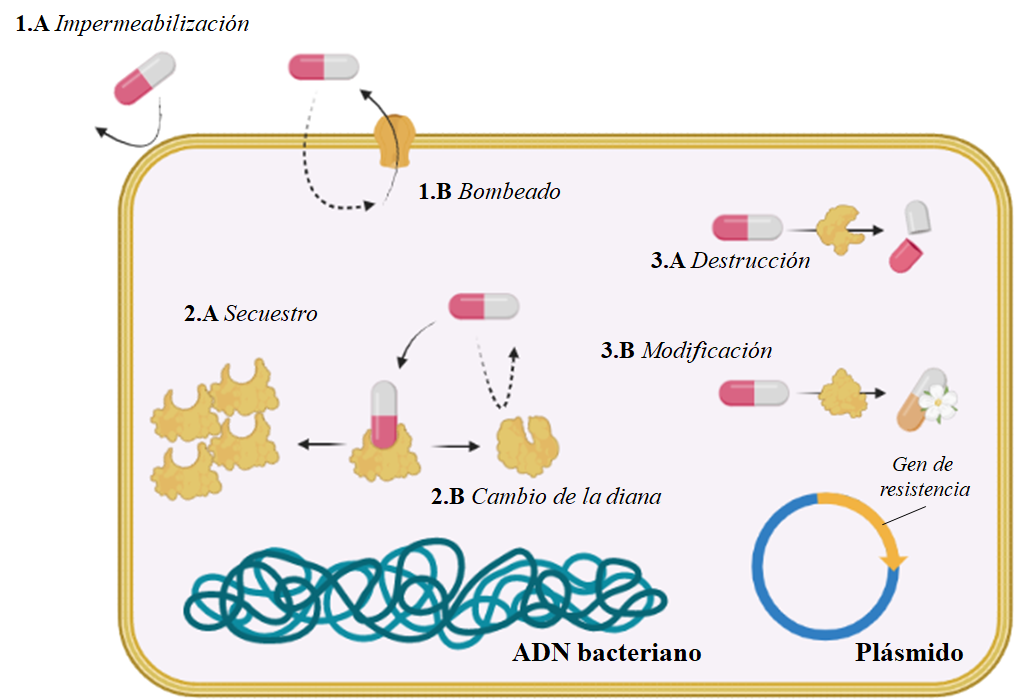
- Reducir la exposición al AB: Esta estrategia se basa en que las bacterias eviten que el AB se acumule dentro de ellas. Para conseguirlo algunas cambian la composición de su “piel” para hacerse impermeables a él (1A), y otras desarrollan sistemas de bombeo, denominados efflux (1B), escupiendo al exterior el agente dañino.
- Cambio de la diana: Un AB puede unirse a una molécula vital para la bacteria (diana), bloqueando su función o dañándola, y por lo tanto provocar la muerte de ésta. La bacteria, para defenderse puede aumentar el número de dianas (2.A); cambiar ligeramente la forma de la diana para que siga siendo funcional pero que el AB no se una a ella (2.B), haciendo el AB completamente inofensivo; o producir moléculas que protejan el lugar de unión del fármaco.
- Desactivación: La bacteria puede desarrollar enzimas que rompan o destruyan el fármaco (3.A), haciéndolo inactivo o que cambien su forma (3.B) y lo hagan inofensivo.
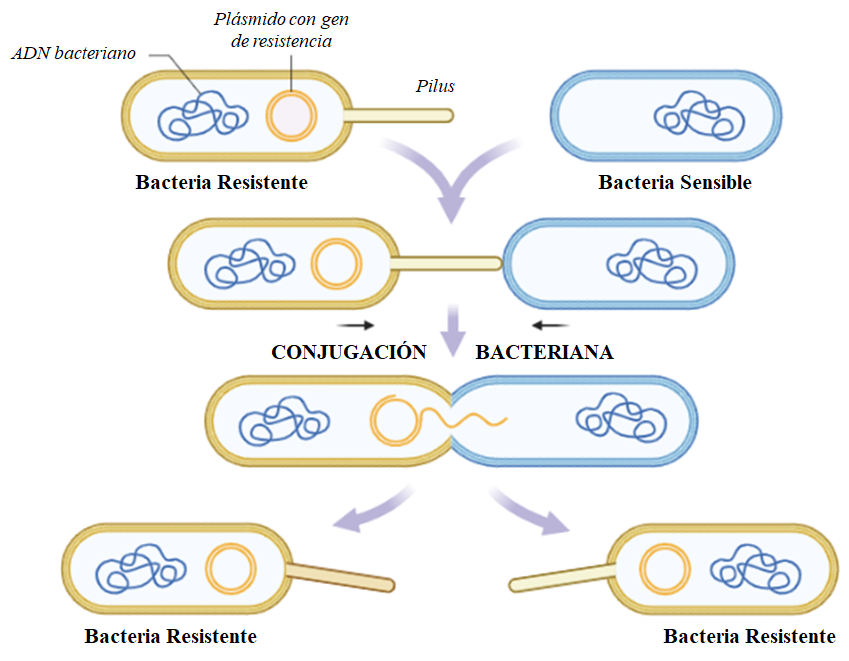
Constantemente se están descubriendo nuevas estrategias de resistencia y nuevos genes que otorgan esta capacidad a bacterias patógenas. Estas habilidades pueden surgir de forma aleatoria en el ADN de las bacterias, por medio de mutaciones, y además pueden diseminarse entre indivíduos. Una forma de esta diseminación son los pili (plural de pilus) mencionados anteriormente. Con ellos las bacterias que posean en un plásmido con la información para poder resistir a un AB, pueden copiarlo y pasarlo a sus compañeras sean o no de la misma especie para que éstas también puedan resistir (Figura 3).
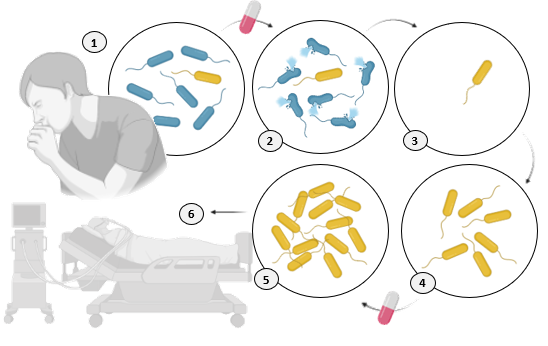
La generación de resistencias es un evento totalmente natural. El problema está en que éstas están apareciendo muchísimo más rápido de los previsto debido al mal uso y abuso de los AB por parte de: los sanitarios, por recetar cuando no son necesarios; la industria ganadera por usarlos de forma indiscriminada para prevención de enfermedades y engorde (prohibido en la UE desde 2006); los pacientes, por no respetar las pautas de administración fijadas (o incluso a veces automedicarse), etc. En el caso de los pacientes esto suele ocurrir a menudo por desconocimiento, y es que se piensa que los AB sirven para tratar cualquier infección, cuando en realidad solo son útiles contra bacterias, y no para hacer frente a infecciones provocadas por virus, hongos o parásitos (Figura 4).

Empezamos a perder batallas
Hoy en día mueren más de 700.000 personas anualmente a causa de infecciones multirresistentes. La OMS estima que de no cambiar nuestros hábitos, en 2050 podrían causar más de 10 millones de muertes anuales a nivel global, superando así al cáncer y enfermedades cardiovasculares como primera causa de muerte en el mundo.
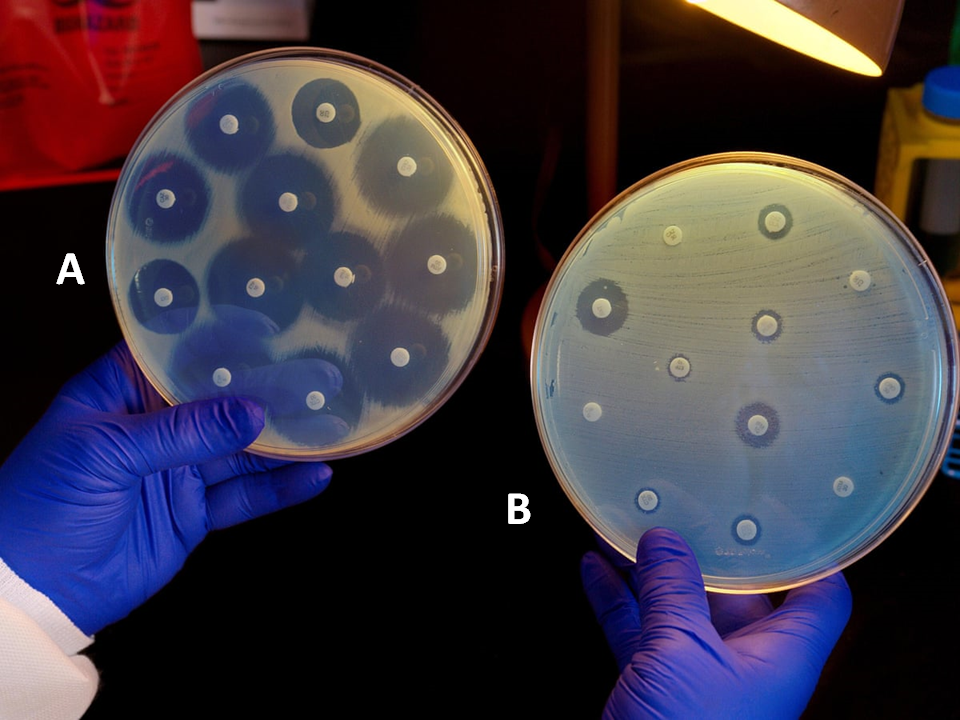
Algunas de las bacterias que nos colonizan actualmente ya son resistentes, y de hecho muchos fármacos se administran junto con inhibidores de resistencias directamente para que sean eficaces. Como ejemplo de ello tenemos la amoxicilina con el ácido clavulánico (el famoso Augmentine ®), empleado a menudo para tratar múltiples infecciones causantes de amigdalitis, cistitis, pneumonías, etc. siempre y cuando éstas sean bacterianas (Figura 5). La amoxicilina (un tipo de penicilina) es un AB que destruye la pared de las bacterias, pero éstas han desarrollado una molécula llamada β-lactamasa que destruye a su vez la amoxicilina. El ácido clavulánico evita que esto ocurra, inhibiendo a la β-lactamasa y permitiendo así que la amoxicilina ejerza su acción.
Por poner un ejemplo de un uso indebido de este fármaco en concreto podemos destacar: por parte del paciente, no terminar la pauta recomendada por el sanitario o por auto-diagnosticarse y tratarse con este AB; o por parte de profesionales, cuando por ejemplo algunos dentistas (aunque con buena fe) recetan de forma profiláctica amoxicilina y ácido clavulánico para evitar infecciones tras un procedimiento en la boca, cuando en realidad sólo deberían recetarlos en indicados procedimientos y en determinados pacientes.
¿Cómo evitar el desastre?
“Es mejor prevenir que curar”; la mejor forma de defenderse de un patógeno es evitar el contacto con éste en un primer lugar. Algo bueno que ha traído la pandemia de la COVID-19 es la conciencia sobre la importancia de los buenos hábitos de higiene, y seguir con ellos después de la pandemia es una vital para preservar una buena salud y posibles infecciones de toda clase, también de bacterias resistentes. Dentro de la prevención, también será clave en un futuro el desarrollo de vacunas que prevenga infecciones de bacterias resistentes en la población. Incluso debería extenderse el uso de la vacunación y medidas más estrictas de higiene en algunos sectores de la ganadería para así evitar el abuso de antibióticos.
El apoyo a la investigación es muy importante, desde la ciencia básica hasta la traslacional. La ciencia básica con el estudio de las bacterias resistentes nos ayudará a entender mejor sus mecanismos de resistencia y por tanto a dilucidar nuevas estrategias de ataque. Mientras que la ciencia traslacional nos ayudará al desarrollo de nuevos fármacos seguros y eficaces en la eliminación de patógenos multirresistentes.
La lucha contra las resistencias a los antibióticos requiere del compromiso, concienciación y coordinación de múltiples actores: los médicos, farmacéuticos, enfermeros, dentistas, científicos, pacientes, e incluso de sectores como la ganadería, la industria y el tratamiento de aguas y residuos. Hay que destacar que el uso responsable de los AB nos concierne a todos ya que se trata de microorganismos vivos que pueden desarrollarse y transmitirse tanto en la naturaleza como dentro del cuerpo humano. Es decir, que un individuo haga un mal uso de los AB, aparezca una nueva bacteria resistente y haya una cadena de transmisión puede provocar que ese AB ya no sirva más para tratar infecciones. No seamos nosotros mismos los que nos quitemos estas armas tan efectivas y costosas de crear y producir (Figura 6).
Cabe destacar que además de las bacterias, hongos, parásitos y virus, también están sujetos a leyes evolutivas de selección biológica y que por tanto también pueden generar resistencias a antifúngicos, antiparasitarios y antivirales, por lo que su uso también debe ser racional.
El mundo postantibióticos y las armas del futuro
Siguiendo la tendencia actual, el mundo postantibióticos acabará llegando. Pero en nuestras manos está que éste llegue más tarde y de estar preparados para cuando ocurra, para que así el mundo postantibióticos se parezca lo menos posible al preantibióticos, donde habría que lamentar la muerte de millones de personas anualmente por infecciones hoy en día fácilmente tratables.
Existen grupos de investigación que están desarrollando nuevos tratamientos que eventualmente puedan sustituir a los antibióticos empleados actualmente. Entre ellos tenemos: Antibióticos de nueva generación que por ejemplo se unan por más de dos sitios distintos a su diana en una bacteria, haciendo así que la probabilidad de que se desarrolle una bacteria resistente sea aún menor; vacunas terapéuticas, desarrollo de vacunas que además de prevenir las infecciones ayuden en su eliminación; la inoculación de anticuerpos monoclonales para la terapia (inmunidad pasiva), técnica que sería especialmente útil para tratar a pacientes con débiles sistemas inmunes y en los que las vacunas serían poco efectivas; el uso de bacteriófagos, virus que sólo atacan a bacterias (fagoterapia); trasplantes de microbiota, colonizar previamente un paciente con bacterias comensales y simbióticas, para no dejar espacio a las patógenas para establecerse; etc.
Agradecimientos
A Uxue Pérez, doctoranda en microbiología, y Andrea Juandeaburre, odontóloga, por su asesoramiento y revisión del texto.
Imágenes
- Figura 0: https://www.ft.com/content/8af200f0-54b4-11e6-9664-e0bdc13c3bef
- Figura 4: Tumblr (adaptado).
- Figura 5: https://www.theguardian.com/society/2019/sep/11/bacteria-developing-new-ways-resist-antibiotics-doctors-warn.
- El resto de figuras son de elaboración propia gracias a la plataforma BioRender.
Fuentes y bibliografía para saber más
- https://www.weforum.org/agenda/2018/03/the-50-most-important-life-saving-breakthroughs-in-history.
- ttps://www.who.int/news/item/29-04-2019-new-report-calls-for-urgent-action-to-avert-antimicrobial-resistance-crisis.
- Jessica M. A. Blair, et al. Molecular mechanisms of antibiotic resistance. Nat Rev Microbiol. 2015;13(1):42–51.
- Micoli F, et al. The role of vaccines in combatting antimicrobial resistance. Nat Rev Microbiol. 2021;19(5):287–302.
- Capítulo 17: Agentes Antibacterianos. Murray, et al. (2013). Microbiología Médica. 7ºEd. Elsevier. Pp. 165-173.
- Capítulo 23: Fármacos Antibacterianos y Resistencias. Sherry, et al. (2010). Microbiología Médica. 5ºEd. McGrawHill. Pp. 310-330.